Alzheimer và gánh nặng mà bệnh Alzheimer gây ra
Bệnh Alzheimer (AD) là một trong các nguyên nhân chính dẫn đến tình trạng suy giảm trí nhớ và giảm khả năng tư duy, đặc biệt là ở người cao tuổi. Bệnh khởi phát âm thầm và diễn biến trong thời gian dài, người bệnh mất khả năng tự chủ và dần phụ thuộc hoàn toàn vào sự chăm sóc của gia đình cũng như nhân viên y tế.
Chính vì vậy, bệnh Alzheimer tạo ra gánh nặng kinh tế rất lớn cho xã hội. Theo số liệu của hiệp hội Alzheimer Hoa Kỳ, chi phí cho bệnh nhân Alzheimer và bệnh nhân suy giảm trí nhớ do các nguyên nhân khác vào khoảng 321 tỷ USD năm 2022 và có thể tăng lên 1 nghìn tỷ vào năm 2050. Alzheimer cũng là một trong 10 nguyên nhân gây tử vong hàng đầu ở người cao tuổi, tỷ lệ bệnh nhân Alzheimer trên 65 tuổi tử vong ở Mỹ là 10%. Việt Nam là một trong số những quốc gia có tỷ lệ già hóa nhanh nhất trong khu vực Châu Á. Đến năm 2050, số người từ 60 tuổi trở lên ở Việt Nam được ước đoán khoảng 29 triệu người, gấp đôi so với số liệu hiện nay (Hình 2).
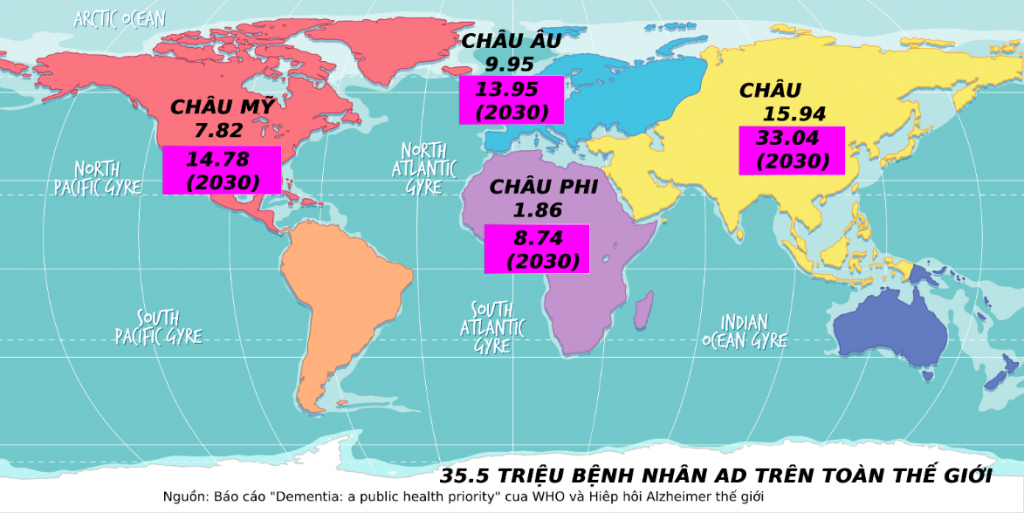
Hình 2. Dự đoán phân bố bệnh nhân Alzheimer trên thế giới: từ hiện tại đến năm 2030
Mặc dù, không có báo cáo đầy đủ về số lượng người mắc bệnh Alzheimer nhưng do đặc điểm của bệnh phổ biến ở người cao tuổi, số lượng bệnh nhân Alzheimer ở Việt Nam cũng sẽ có chiều hướng tăng nhanh trong những năm tới. Việt Nam là một trong những quốc gia có tốc độ già hóa nhanh nhất ở châu Á. Đến năm 2050, số người từ 60 tuổi trở lên sẽ là gần 29 triệu người, hơn gấp đôi so với hiện nay. Mặc dù chưa có thống kê đầy đủ về tổng số bệnh nhân Alzheimer ở Việt Nam, chúng ta có thể hình dung số lượng bệnh nhân ở Việt Nam sẽ rất lớn. Nếu tương đương với tỷ lệ khoảng 10% người từ 65 tuổi trở lên mắc Alzheimer ở Mỹ, số người Việt Nam sẽ sống với Alzheimer là gần ba triệu vào năm 2050 – một con số khổng lồ! Điều này sẽ tạo áp lực lên nền kinh tế và gây hậu quả nghiêm trọng cho xã hội. Do đó, việc phát triển các tác nhân mới có thể chữa trị, điều trị và phòng ngừa Alzheimer hoặc cải thiện chất lượng cuộc sống của bệnh nhân Alzheimer là cấp bách.
Nguyên nhân gây bệnh Alzheimer
Nguyên nhân gây bệnh Alzheimer cho đến nay vẫn chưa được xác định chính xác (Hình 3). Mặc dù vậy một số giả thuyết về cơ chế bệnh sinh được chấp nhận rộng rãi, như sự suy giảm tổng hợp acetylcholin, sự tích tụ các amyloid β peptide – mảng amyloid(Aβ), tích tụ protein tau – đám rối thần kinh, kèm theo căng thẳng oxy hóa – stress oxy hóa, ảnh hưởng của các ion kim loại và nhiều yếu tố khác. Trong đó, giả thuyết về sự suy giảm hệ cholinergic – hệ phản ứng với acetylcholin, là đề xuất đầu tiên và một số chất ức chế enzym acetylcholin esterase (AChE) đã được sử dụng làm thuốc như tacrin, donepezil, galantamin, rivastigmin. Tuy nhiên, các thuốc ức chế AChE hiện nay chỉ làm chậm sự tiến triển của tình trạng suy giảm nhận thức, không điều trị khỏi bệnh. Hướng nghiên cứu tiếp theo trong điều trị bệnh Alzheimer dựa trên giả thuyết về các amyloid β peptide là ức chế sự hình thành Aβ, ức chế sự tích tụ Aβ, loại bỏ các mảng Aβ và liệu pháp miễn dịch. Mặc dù giả thuyết liên quan tới Aβ được biết đến với nhiều chứng cứ khoa học và rất nhiều tác nhân kháng bệnh Alzheimer tiềm năng đã được công bố theo hướng này, nhưng hầu hết các tác nhân đều không cho thấy hiệu quả trên lâm sàng, ngoại trừ loại thuốc tên là aducanumab.
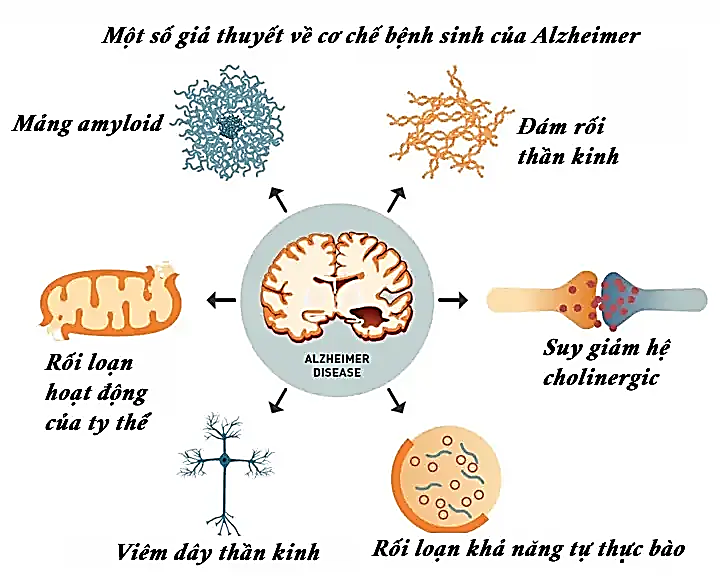
Hình 3. Một số giả thuyết về cơ chế gây bệnh Alzheimer
Căng thẳng oxy hóa, tăng lên ở những bệnh nhân Alzheimer, có thể gây ra sản xuất quá mức các peptide Aβ. Các peptide Aβ sản xuất quá mức có thể kết hợp thành các dạng oligomer độc hại dẫn đến khởi động các quá trình gốc tự do gây ra thay đổi cấu trúc và chức năng của protein, các điều kiện bệnh lý, tổn thương và apoptosis của tế bào thần kinh.
Bên cạnh đó, sự tham gia của các ion kim loại trong cơ chế bệnh sinh của Alzheimer được chứng minh thông qua các liên hệ chặt chẽ giữa bệnh Alzheimer và sự rối loạn điều hòa các ion kim loại. Các mảng amyloid trong não của bệnh nhân Alzheimer tích lũy đồng (Cu), kẽm (Zn) và sắt (Fe) ở mức cao hơn não người bình thường lần lượt là 5,7; 3,1 và 2,8 lần. Do đó, các tác nhân khóa ion kim loại cũng là một trong số các chất có tiềm năng điều trị bệnh Alzheimer. Tuy nhiên, việc thiết kế, phát triển các tác nhân khóa kim loại kháng Alzheimer gặp rất nhiều thách thức do ion kim loại đóng nhiều vai trò quan trọng khác trong cơ thể. Cụ thể, một số yếu tố cần được đảm bảo trong cấu trúc của các tác nhân như: khả năng thấm qua hàng rào máu não, chọn lọc với ion Cu2+ để tránh tương tác với ion sắt và kẽm vốn có trong nhiều enzym quan trọng khác của cơ thể, chọn lọc với các enzym và metalloprotein (dùng để chỉ một protein có sự liên kết/bao bọc ion kim loại) liên quan đến cơ chế gây bệnh Alzheimer. Nhìn chung, các chất khóa ion Cu2+ thường là dẫn chất của các khung hydroxyquinolin, aminoquinolin, tatraazamacrocyles, aminophenol, aminopyridin, bis(thiosemicarbazo-nato), peptid, v.v. (Hình 4).
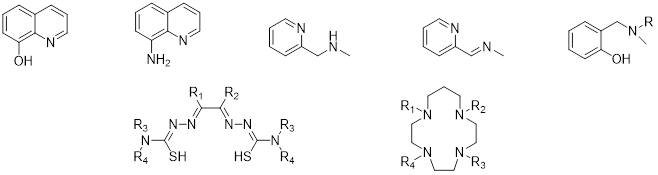
Hình 4. Cấu trúc một số khung cấu trúc thường gặp của các phối tử với ion Cu2+ hướng kháng Alzheimer
Cho đến nay, tác động làm tăng nồng độ acetylcholin thông qua việc ức chế enzym AChE vẫn được coi là hướng nghiên cứu có hiệu quả nhất trong việc tìm kiếm các thuốc mới điều trị AD. Thông qua kỹ thuật chụp hình tinh thể X-ray, cấu trúc của enzym AChE cũng như vai trò của các vị trí tác dụng trên enzym đã được phân tích và xác định. Nhìn chung, enzym AChE được tạo bởi 2 tiểu đơn vị đồng nhất, mỗi tiểu đơn vị có 1 vị trí liên kết chứa 1 trung tâm hoạt động, 1 kênh emzym và 1 trung tâm ngoại vi. Khi tác động vào vị trí trung tâm ngoại vi không chỉ làm tăng áp lực của các chất ức chế với enzym mà còn có tác dụng ức chế sự hình thành các Aβ. Do đó, việc thiết kế các chất ức chế AChE mới có thêm hợp phần cấu trúc có khả năng tương tác với vị trí ngoại vi, thiết kế các cấu trúc đa chức năng, là một xu thế mới kỳ vọng mang đến không chỉ một mà nhiều tác dụng trong điều trị AD.
Các chiến lược phòng và điều trị Alzheimer
Các chiến lược hiện tại cho phòng và trị bệnh Alzheimer dựa trên Aβ bao gồm ức chế sản xuất Aβ, chống Aβ tập hợp, làm sạch Aβ và liệu pháp miễn dịch. Mặc dù có nhiều bằng chứng ủng hộ cho giả thuyết Aβ, nhưng cũng có những hạn chế. Mặc dù nhiều ứng viên thuốc đã bước vào giai đoạn lâm sàng, ngoại trừ aducanumab, tất cả các ứng viên thuốc (các thử nghiệm lâm sàng từ năm 2002 đến 2012) nhắm vào giả thuyết Aβ đã thất bại trong các thử nghiệm lâm sàng giai đoạn III. Mới đây, vào tháng 6 năm 2021, FDA đã phê duyệt aducanumab như là một phương pháp điều trị cho AD vì nó giúp làm giảm Aβ tích tụ. Mặc dù aducanumab làm giảm tích tụ Aβ, có tranh cãi rằng các thử nghiệm lâm sàng đã không chứng minh được nó có cải thiện lâm sàng cho bệnh nhân AD. Một số tác giả đã cho rằng các loại thuốc đã thất bại không làm giảm đáng kể Aβ ngoại bào hoặc nồng độ Aβ thấp không tương ứng với AD. Hơn nữa, theo giả thuyết Aβ, việc loại bỏ Aβ có thể gây ra tác dụng phụ nghiêm trọng do vai trò sinh lý của Aβ. Tóm lại, các tác nhân chống Aβ vẫn là ứng viên chính cho việc phòng và trị bệnh Alzheimer trong tương lai gần.
Các dẫn chất tetrazole hướng tới điều trị Alzheimer
Tetrazole là một lớp hợp chất hữu cơ dị vòng phổ biến có sự chú ý đặc biệt nhờ cấu trúc và tính chất hóa học độc đáo, cùng với một loạt các hoạt tính dược lý như tác dụng chống co giật, kháng sinh, chống dị ứng, hạ huyết áp và nhiều ứng dụng khác. Nhờ vào các tính chất hóa học và sinh học quan trọng, những tiến bộ gần đây trong việc tổng hợp các dẫn chất tetrazole đang tập trung vào vai trò của chúng trong điều trị các bệnh thần kinh, trong đó có bệnh Alzheimer.
Tetrazole là một vòng 5 cạnh (khung dị vòng trong Hình 5) bao gồm bốn nguyên tử nitơ và một nguyên tử carbon không bão hòa, được lần đầu tiên báo cáo về việc tổng hợp thành công bởi Bladin vào năm 1885. Trong những năm qua, khung tetrazole thu hút sự quan tâm trong hóa dược vì các đặc tính và cấu trúc độc đáo của nó.
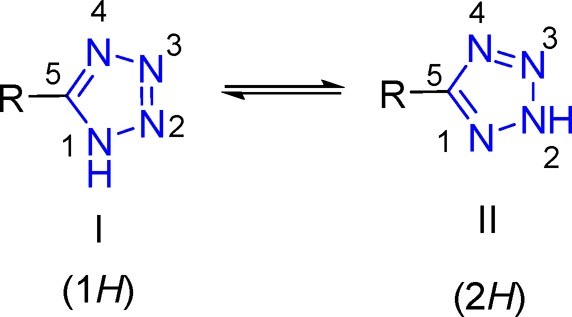
Hình 5. Phản ứng đồng phân hóa hỗ biến (tautome hóa) của các dẫn chất tetrazole
Cấu trúc vòng tetrazole cho phép thiết kế và tổng hợp các dẫn chất là đồng phân ổn định sinh học với nhiều ứng dụng trong điều trị bệnh như chống virus, bệnh lao, sốt rét, chống nấm, chống ung thư, chống vi khuẩn, bảo vệ hệ thần kinh, hạ huyết áp, v.v. Ứng dụng triển vọng của các dẫn chất tetrazole có thể được minh họa bởi các loại thuốc được bán trên thị trường như cenobamate – thuốc sử dụng để điều trị cơn co giật. Hoạt động của các dẫn chất tetrazole đã được mô tả thông qua khả năng ức chế các mục tiêu và enzyme liên quan đến các rối loạn thần kinh. Các bệnh lý liên quan đến rối loạn thần kinh gây ra sự suy giảm hoặc suy thoái sự phát triển của các tế bào thần kinh, dẫn đến chứng mất trí, suy giảm chức năng vận động và chức năng nhận thức trong nhiều vùng não. Theo Tổ chức Y tế Thế giới (WHO), rối loạn thần kinh là nguyên nhân chính thứ hai gây tử vong và bệnh tật, bao gồm các căn bệnh nguy hiểm như Alzheimer, trầm cảm, động kinh, Parkinson, thần kinh tiểu đường, đa xơ cứng, tổn thương tủy sống. Hiện nay, các loại thuốc như rivastigmine, donepezil, memantine, và galantamine cho Alzheimer; pramipexole, piribedil, apomorphine, levodopa, rasagiline, entacapone, selegiline và safinamide cho Parkinson; pregabalin và duloxetine cho thần kinh tiểu đường; cladribine, dimethylfurmate và teriflunomide cho đa sơ cứng động mạch đang có sẵn trên thị trường. Tuy nhiên, các nhược điểm liên quan đến các loại thuốc có sẵn này như sự không hiệu quả trong việc chữa trị tiến triển bệnh và thiếu đặc hiệu, nên cần phát triển các liệu pháp điều trị sáng tạo dựa trên các khung hóa chất mới.
Tầm quan trọng của các dẫn chất tetrazole trong hóa dược và thiết kế thuốc phát sinh từ sự tương đồng về mặt cấu đẳng sinh học (bioisosteric) với các nhóm carboxylic acid và amide cùng với tính ổn định chuyển hóa và các tính chất hóa – lý có lợi khác. Một ví dụ là dựa trên đặc tính này, các dẫn chất mang khung (pyridine-2-yl)tetrazol đã được tổng hợp với sự hiện diện của các nhóm acid, ester và amide và được đánh giá có hiệu quả cao đối với hiệu ứng ức chế enzyme acetylcholinesterase (AChE). Nhiều nghiên cứu như vậy nhấn mạnh tiềm năng của các dẫn chất tetrazole như một liệu pháp và chiến lược điều trị triển vọng cho bệnh nhân Alzheimer.
Trong dự án “Thiết kế, tổng hợp và đánh giá tác dụng sinh học của các dẫn chất Tetrazol đa chức năng mới hướng dùng điều trị bệnh Alzheimer” do Quỹ VinIF tài trợ vào năm 2022, nhóm nghiên cứu chúng tôi dự kiến thiết kế các cấu trúc đa chức năng mới, tiềm năng trong điều trị Alzheimer có chứa một phần cấu trúc mang khung tetrazol hướng đến tương tác vào trung tâm hoạt động và một phần cấu trúc hướng đến tương tác vào vị trí ngoại vi. Cầu nối giữa hai hợp phần cấu trúc này sẽ được khảo sát sự thay đổi cũng như chèn thêm các nhóm chức có khả năng tạo phức với ion kim loại nhằm tăng cường khả năng tương tác đa đích của hợp chất. Dự án kỳ vọng sẽ tạo ra các hợp chất tetrazol đa chức năng mới có hoạt tính tốt giúp chống lại sự tiến triển của bệnh Alzheimer , từ đó mang đến một liệu pháp điều trị hiệu quả và mang lại nhiều lợi ích cho các bệnh nhân Alzheimer cũng như toàn xã hội.
Tác giả: PGS.TS. Trần Phương Thảo, Trường Đại học Dược Hà Nội.
Tổng hợp và biên tập: Quỹ đổi mới sáng tạo Vingroup (VinIF).
Tài liệu tham khảo
1. Better M. A. (2024). Alzheimer’s disease facts and figures. Alzheimer’s Dement, 20, 3708-3821.
2. Woźniak, Kinga, et al. Alzheimer’s Disease-A Comprehensive Review. Journal of Education, Health and Sport 56 (2024): 195-209.